TECHiJET QS-P (iniettore senza ago per insulina U100)
Dettaglio
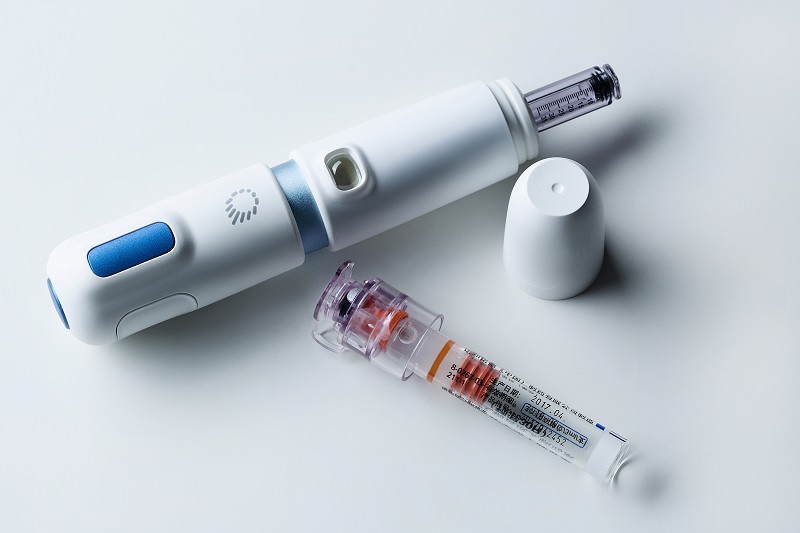
L'iniettore senza ago QS-P è progettato per iniettare farmaci sottocutanei come insulina, ormone della crescita umano, anestetico locale e vaccino.Per ora QS-P è stato approvato per iniettare insulina e ormoni della crescita umani in Cina.L'iniettore senza ago QS-P è un dispositivo alimentato a molla, utilizza un'alta pressione per rilasciare il farmaco liquido da un micro orifizio per creare un flusso liquido ultrafine che penetra istantaneamente dalla pelle al tessuto sottocutaneo.
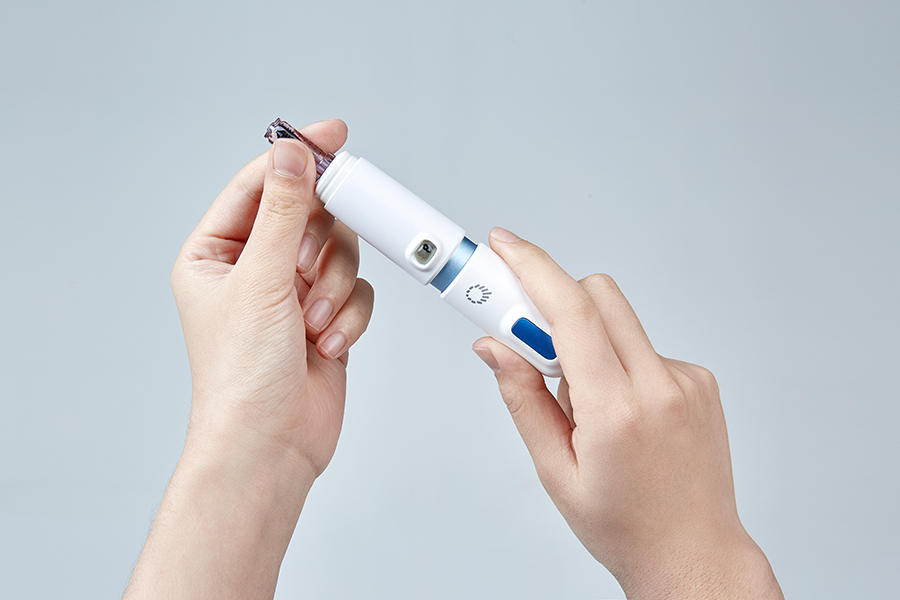
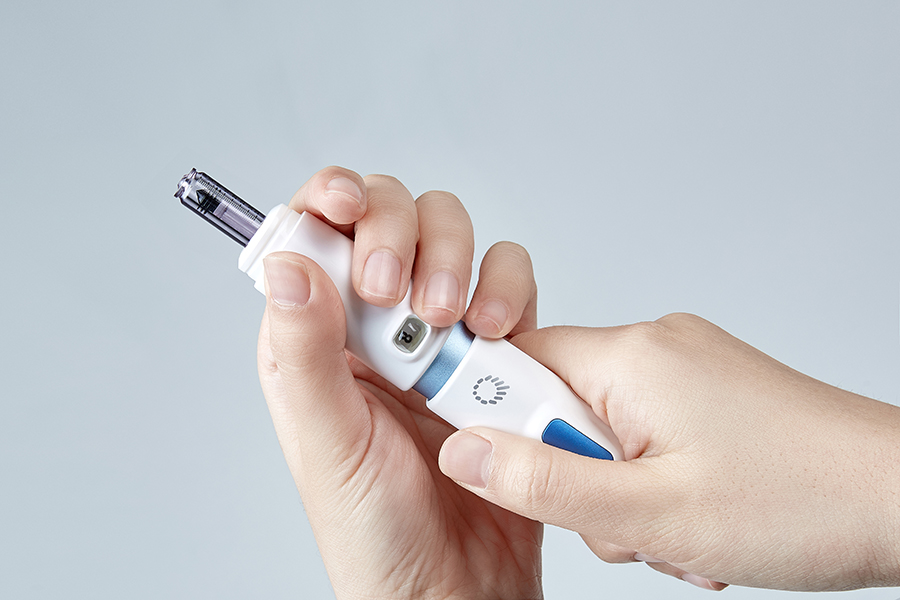
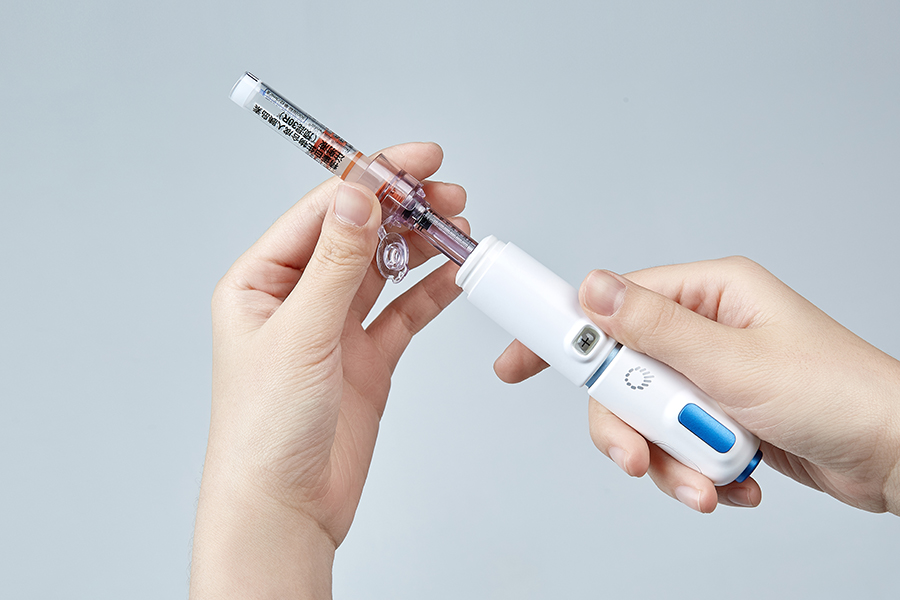
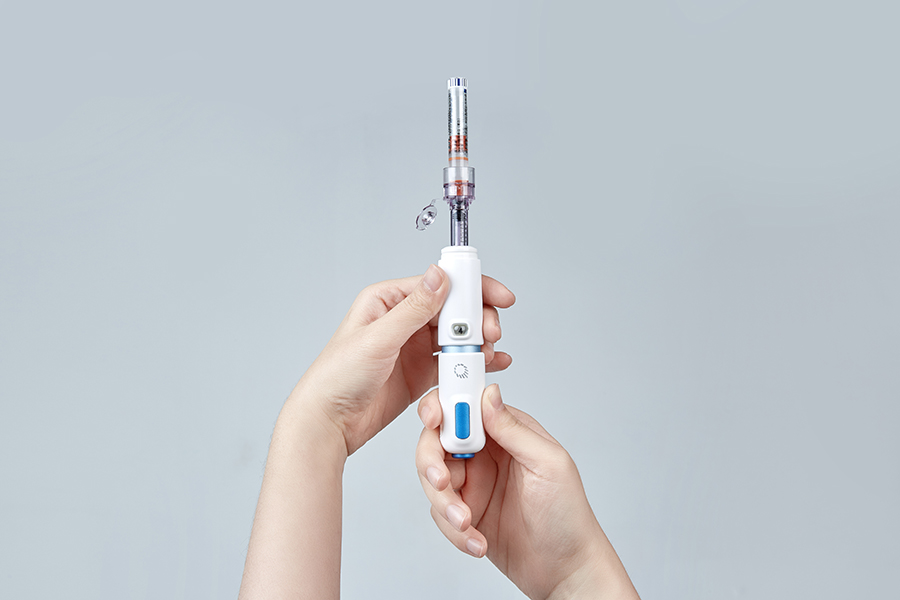
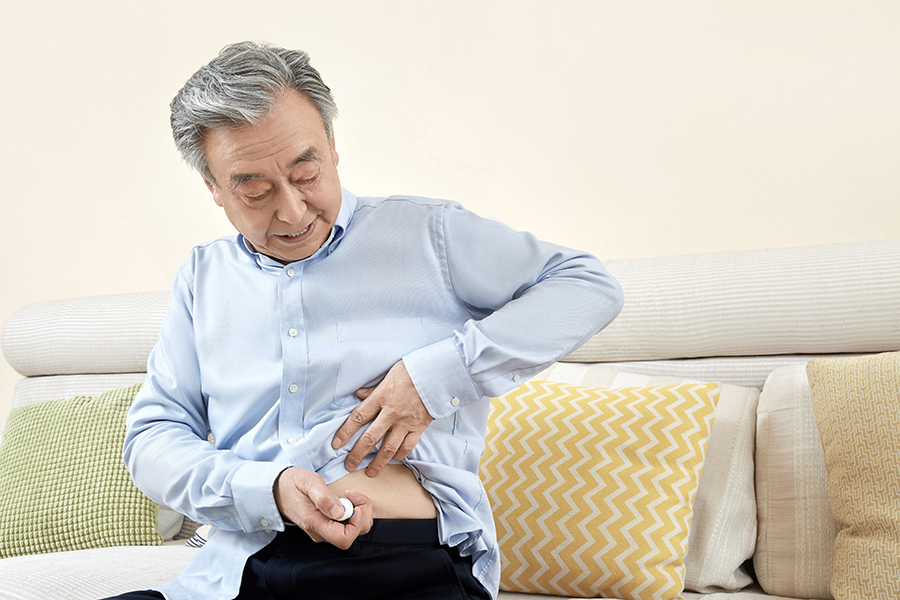
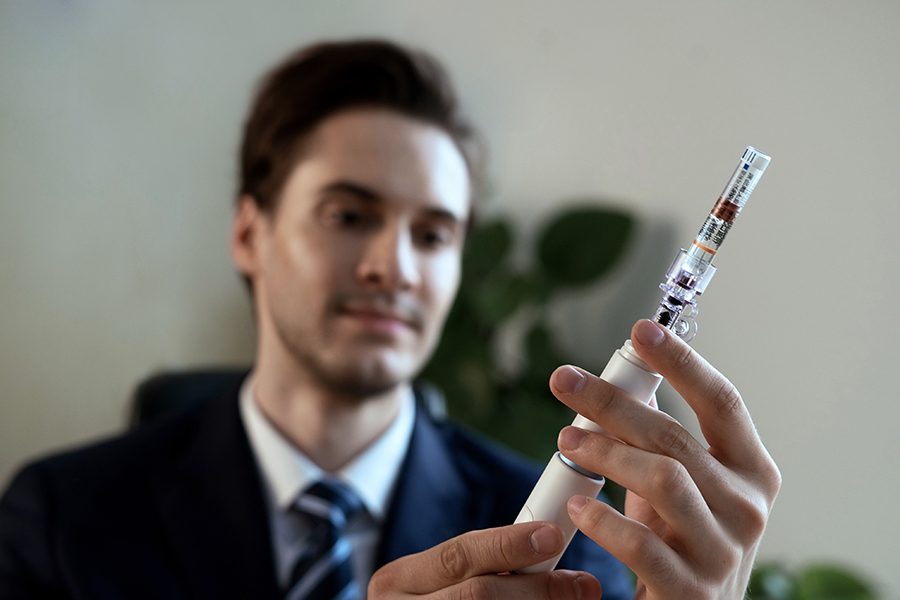
Il QS-P è l'iniettore senza ago di seconda generazione dopo QS-M, il concetto di design è portatile ed è molto facile da mettere in tasca o in una piccola borsa.Un altro concetto di questo design è la leggerezza, il peso di QS-P è inferiore a 100 grammi.Quinovare spera che i bambini o gli anziani possano usarlo da soli.Le operazioni che utilizzano l'iniettore QS-P sono comodamente facili da seguire;prima caricare il dispositivo, secondo estrarre il farmaco e scegliere il dosaggio e terzo iniettare il farmaco.Questi passaggi possono essere appresi entro 10 minuti.Altri iniettori senza ago sono costituiti da due parti diverse, l'iniettore e la scatola di pressione (scatola di ripristino o caricatore di movimentazione).Per quanto riguarda QS-P, è un iniettore di design tutto in uno, quindi è più comodo da usare.Il terzo concetto di design è il calore, la maggior parte delle persone sente freddo o dolore o ha paura degli aghi, abbiamo fatto del nostro meglio per progettare il nostro iniettore in modo che sembri caldo e non assomigli a un iniettore.Volevamo che i clienti potessero usare comodamente l'iniettore e avere fiducia ogni volta che lo usano.Per le sue caratteristiche e il suo design QS-P ha ottenuto il Good Design Award del 2016, il Golden Pin Design Award del 2019 e il Red Star Design Award del 2019.
QS-P è stato sviluppato nel 2014, abbiamo lanciato QS-P sul mercato lo scorso 2018 in Cina, la sua capacità della fiala è di 0,35 ml e l'intervallo di dosaggio è compreso tra 0,04 e 0,35 ml.QS-P ha ottenuto il marchio CFDA (China Food and Drug Association), CE e ISO13485 nel 2017.